Sobre este modelo de Mapa Conceitual de Ligação Química
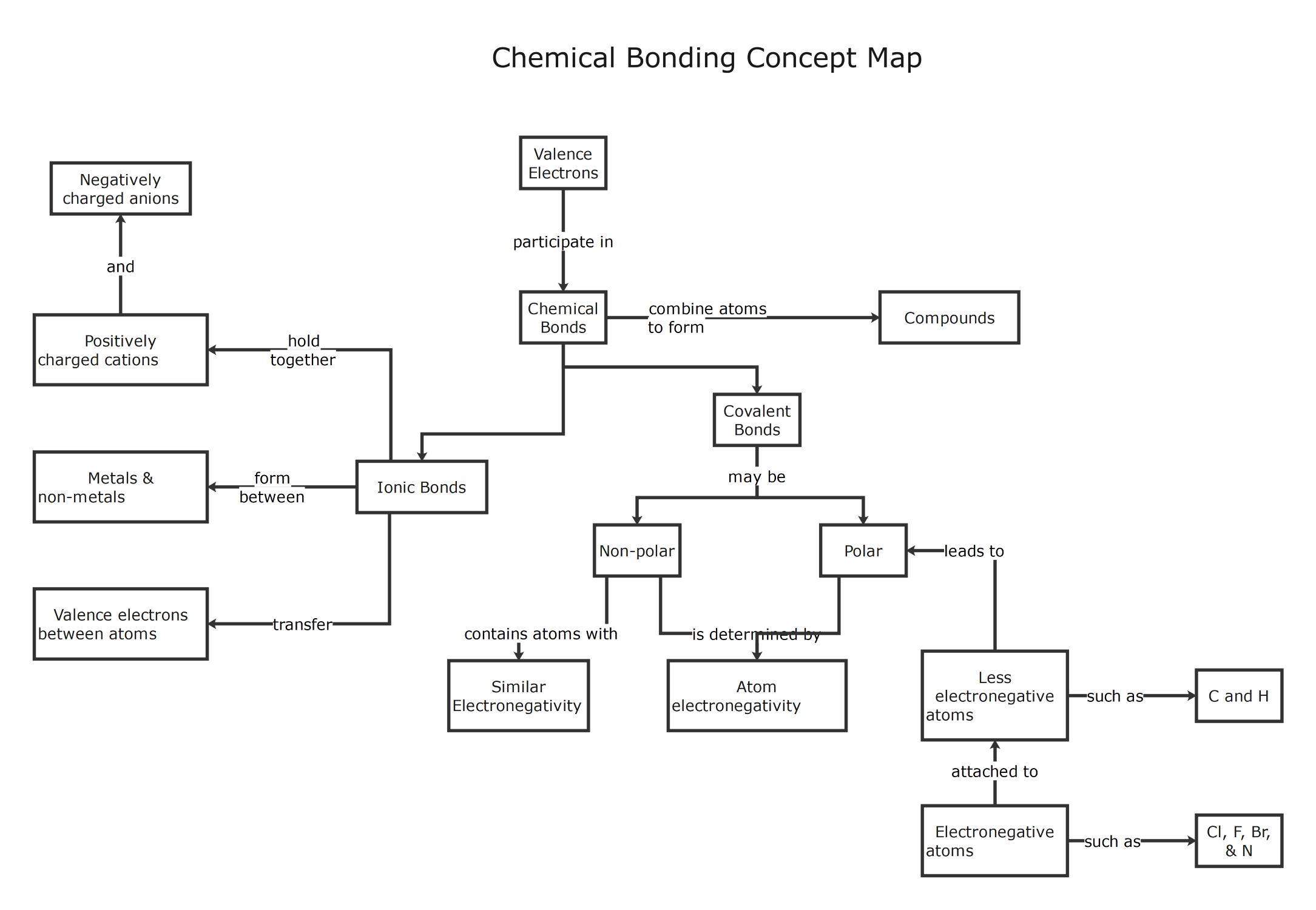
Este modelo fornece um resumo visual claro das maneiras como os átomos interagem através de elétrons de valência. Ele ajuda estudantes e educadores a mapear as diferenças entre ligações iônicas e covalentes, destacando características-chave como eletronegatividade e carga.
Ligações Químicas e Elétrons de Valência
Ligações químicas são formadas quando átomos interagem através de seus elétrons mais externos para alcançar estabilidade. Este processo combina diferentes átomos para criar compostos complexos que são os blocos de construção de toda matéria encontrada no universo.
- Elétrons de Valência
- Ligações Químicas
- Compostos
Ligações Iônicas e Transferência de Elétrons
Ligações iônicas ocorrem quando elétrons são transferidos entre átomos, geralmente envolvendo metais e não-metais. Esta atração mantém íons de cargas opostas unidos para formar estruturas estáveis que são frequentemente encontradas em vários sais comuns e minerais.
- Cátions carregados positivamente
- Ânions carregados negativamente
- Metais e não-metais
- Transferência de elétrons de valência
Ligações Covalentes e Eletronegatividade
Ligações covalentes envolvem o compartilhamento de elétrons entre átomos em vez de uma transferência completa. A natureza deste compartilhamento depende fortemente da eletronegatividade, que determina se a ligação resultante é classificada como polar ou não-polar.
- Ligações Covalentes Polares
- Ligações Covalentes Não-polares
- Eletronegatividade do átomo
- Eletronegatividade semelhante
Características e Exemplos de Ligações Polares
Ligações polares criam distribuição desigual de elétrons quando um átomo eletronegativo puxa elétrons para si. Esta seção destaca elementos comuns envolvidos nestas ligações, como hidrogênio e carbono emparelhados com elementos halogênios altamente reativos.
- Átomos menos eletronegativos (C e H)
- Átomos eletronegativos (Cl, F, Br e N)
- Compartilhamento desigual de elétrons
Perguntas frequentes sobre este modelo
-
Qual é a diferença entre ligações iônicas e covalentes?
As ligações iônicas se formam quando um átomo cede elétrons para outro, criando íons carregados que se atraem. Isso geralmente ocorre entre metais e não-metais. Em contraste, as ligações covalentes envolvem átomos compartilhando elétrons para permanecerem juntos. Isso ocorre com mais frequência entre átomos não-metálicos. Entender esses dois tipos de ligações é essencial para prever como diferentes substâncias se comportarão.
-
Como a eletronegatividade afeta as ligações químicas?
A eletronegatividade mede quão fortemente um átomo atrai elétrons. Se dois átomos têm valores de eletronegatividade muito diferentes, eles provavelmente formam uma ligação iônica. Se os valores são semelhantes, formam uma ligação covalente não-polar. No entanto, se há uma diferença moderada, forma-se uma ligação covalente polar. Isso cria cargas parciais, que influenciam significativamente as propriedades físicas da molécula resultante.
-
Por que os elétrons de valência são importantes neste mapa conceitual?
Os elétrons de valência são os elétrons específicos localizados na camada mais externa de um átomo. Eles são os principais participantes nas reações químicas e ligações. Como são os mais acessíveis, eles determinam como um átomo irá interagir com seus vizinhos. O mapa conceitual os destaca porque todos os tipos de ligação, sejam iônicas ou covalentes, dependem inteiramente do comportamento desses elétrons.


 Nano Banana Pro
Nano Banana Pro